近日,海洋药物教育部重点实验室李文利课题组揭示了一种全新的tRNA依赖型二酮哌嗪-萜类化合物生物合成机制。2018年10月5日,该研究成果以“Genome mining of cyclodipeptide synthases unravels unusual tRNA-dependent diketopiperazine-terpene biosynthetic machinery” 为题发表于国际权威期刊Nature子刊《自然-通讯》(Nature Communications, DOI: s41467-018-06411-x)。
含有二酮哌嗪(DKPs)骨架的天然产物具有能跨过肠屏障和血脑屏障等特点,是重要的药物先导化合物。DKPs的生物合成分为非核糖体肽合酶(NRPSs)和环二肽合酶(CDPSs)两类。目前报道的DKPs主要是通过NRPS途径合成,而CDPS途径是一种与NRPS截然不同的途径。课题组人员采用基因组采掘技术,从三株链霉菌中发现了3个含有CDPS的同源基因簇dmt1-3。体内实验显示DmtB1是首个以cyclo-(L-Trp-L-Val)为主产物的CDPS,能够合成cyclo-(L-Trp-L-Xaa) (Xaa= Val, Pro, Leu, Ile和Ala) 5个产物,对第二个氨基酸的选择性较低,而DmtB2和DmtB3只产生1-2种环二肽,对第二个氨基酸的选择性较强。采用异源表达手段研究了dmt1-3的编码产物,通过体内基因阻断、互补和高表达等遗传操作解析了各个基因的功能,发现了首个具有底物宽泛性的PSL家族异戊烯基转移酶和通过双键质子化起始环化反应的细菌源膜结合萜环化酶,揭示了tRNA依赖型DKP-萜类化合物生物合成机制(图1)。该发现为采用组合生物合成技术开展DKPs类化合物结构多样性研究提供了重要的科学理论指导。
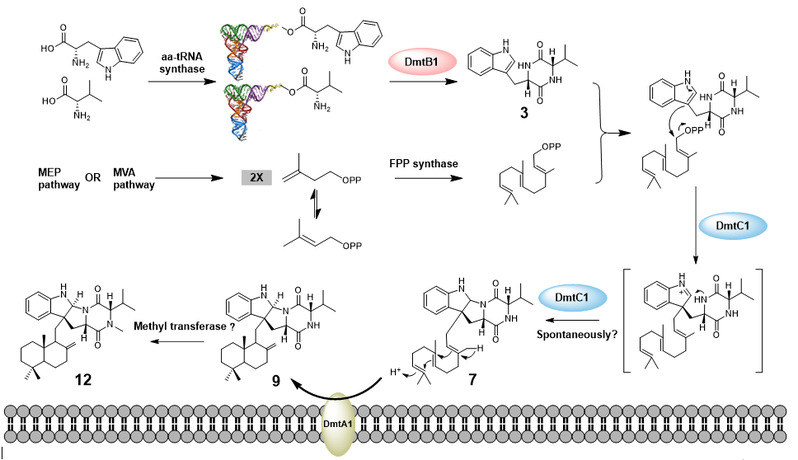
图1 Drimentine生物合成分子机制
海洋药物教育部重点实验室姚婷婷博士和博士研究生刘晶为该论文的共同第一作者,李文利教授为通讯作者。论文共同作者为博士研究生刘增智、李通博士、李花月和车茜副教授,以及朱天骄、李德海和顾谦群教授。研究工作获得了国家自然科学基金、NSFC-山东省政府联合基金等项目的资助。全文链接:https://www.nature.com/articles/s41467-018-06411-x
