单纯疱疹病毒(Herpes simplex virus,HSV)属于疱疹病毒科α病毒亚科,分为HSV-1和HSV-2 两种。HSV-1 主要引起皮肤、口腔粘膜和器官(脑)的感染,HSV-2 主要引起生殖器部位感染。HSV还能引发比较严重的病症,例如疱疹性脑炎在严重情况下可能导致死亡。然而目前临床治疗药物主要为核苷类似物,如阿昔洛韦、伐昔洛韦等,但这些药物存在耐药性及肾毒性等问题。因此,研发针对新作用靶点且安全高效的新型抗HSV 药物十分迫切。HSV 颗粒的表面含有约11 种病毒糖蛋白,其中有4 种糖蛋白(gB,gD,gH 和gL)对于HSV进入宿主细胞是必需的。因此靶向这些糖蛋白的药物能够有效抑制HSV的感染和传播。胍基修饰的化合物具有广泛的抗病毒活性,如流感病毒糖蛋白NA的抑制剂扎纳米为及广谱抗病毒药盐酸胍。因此,胍基修饰的化合物有可能具有HSV的糖蛋白靶向性和抗HSV活性。
基于此,海洋药物教育部重点实验室合成药化室的江涛教授与药理室王伟副教授合作团队利用抗HSV的分子和细胞模型对胍基修饰的嘧啶衍生物进行抗HSV活性筛选,发现了一种嘧啶胍基衍生物5d具有显著的体外抗HSV作用(IC50 < 2.5 μM),相比未修饰的3a提高了超过200倍。5d对HSV-1和HSV-2都具有很好的抑制作用,且优于临床药物阿昔洛韦(IC50 > 9.5 μM)。另外,5d(10 mg/kg/day)腹腔注射给药能够显著提高HSV-1感染小鼠的生存率,降低肺部和脊髓的病毒滴度,减轻肺部和脑部的炎性损伤,优于同剂量的临床药物阿昔洛韦,且未修饰的3a无保护作用。

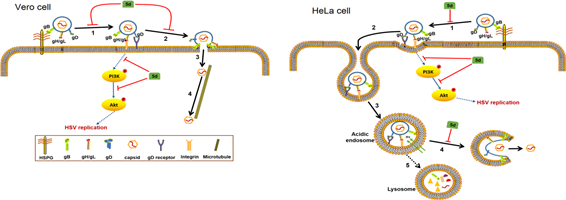
作用机制研究发现化合物5d不仅抑制HSV的吸附过程还可抑制HSV的内吞和膜融合过程。5d定位于细胞核周围区域且与晚期内体和溶酶体存在明显共定位。免疫荧光、DARTS和免疫共沉淀实验表明化合物5d而非未修饰的3a能够特异性地结合HSV的gB蛋白,且分子对接研究表明5d与gB的结合能力远远高于3a。此外,5d还能够显著下调HSV侵染相关的PI3K/Akt信号通路。因此,胍基修饰的嘧啶衍生物5d能够通过靶向结合gB蛋白来抑制HSV的吸附和膜融合过程,并间接干扰PI3K/Akt通路的激活,从而抑制HSV的侵染和复制过程。这为基于胍基修饰的新靶点抗HSV药物的研发提供了物质基础和理论参考。
该研究成果于2019年11月10日在线发表于药理学顶尖期刊British Journal of Pharmacology(药学一区,TOP期刊,IF = 6.583)。
江涛教授和王伟副教授为该研究成果的共同通讯作者,王伟副教授,徐萃婧同学和张建强同学为并列第一作者,于日磊副教授为合作作者。该研究得到了国家自然科学基金、国家基金委-山东省联合基金、国家重点研发计划以及山东省面上基金等项目的资助。
Guanidine Modifications Enhance the Anti-Herpes Simplex Virus Activity of (E, E)-4,6-bis (styryl)-pyrimidine Derivatives in vitro and in vivo. Br J Pharmacol. 2019 Nov 10. doi: 10.1111/bph.14918.
文章链接:https://bpspubs.onlinelibrary.wiley.com/doi/abs/10.1111/bph.14918
