近日,中国海洋大学医药学院、海洋药物教育部重点实验室王杨课题组在药物分子优势骨架的合成新方法方面取得重要进展,相关研究成果以“Catalyst-free and oxidant-free tandem aza-Mannich/cyclization/aromatization of C,N-cyclic azomethine imines with enamides: facile synthesis of 5,6-dihydropyrazolo[5,1-a]isoquinolines”为题,以封面文章(图1)的形式发表于在国际化学领域顶级期刊《Green Chemistry》(IF = 11.034)。

图1. 工作被选为《Green Chemistry》期刊封面文章
含氮杂环广泛存在于天然产物和药物活性分子中。其中异喹啉并吡唑是一类常见的含氮杂环骨架,其广泛应用于医药领域,具有多种生物活性,是许多药物的重要中间体。海洋来源的吡唑类生物碱也含有类似骨架。异喹啉并吡唑骨架的合成方法吸引了化学家们的关注,目前已经发展了包括环加成反应、金属催化的偶联反应、还原胺化反应以及自由基反应等方法用于构建异喹啉并吡唑类结构。这些传统的合成方法需要催化剂、添加剂以及氧化剂来构建骨架中的吡唑环,存在步骤多,普适性差等问题。此外受反应和底物结构的限制,大多数方法只能构建带有特定官能团的异喹啉并吡唑骨架,这给后续产物结构的改造与修饰带来了困难。因此发展一种绿色、高效、普适的合成方法来构建异喹啉并吡唑骨架,对于异喹啉并吡唑衍生物的研究及开发利用具有重要意义。
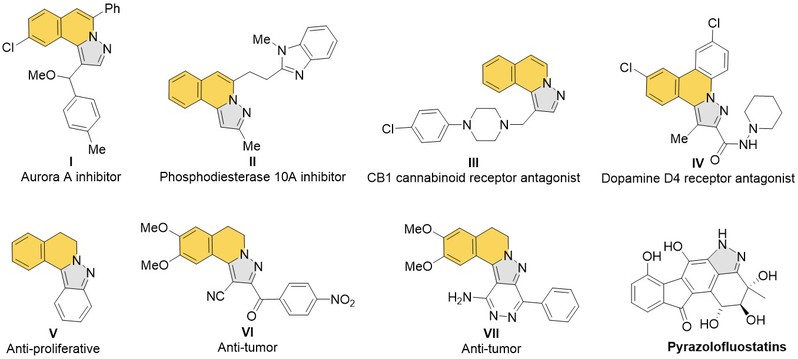
图2. 含有异喹啉并吡唑骨架的药物活性分子及海洋天然产物
王杨课题组从C,N-亚甲胺内盐和烯酰胺出发,通过全新的氮杂Mannich反应/环化/芳香化机理,发展了一种绿色、高效构建异喹啉并吡唑结构的方法。该方法无需添加任何添加剂,且反应条件温和,底物适用范围广,产率高,为异喹啉并吡唑骨架的合成提供了一种全新的思路和策略。烯酰胺作为一种活性烯烃,受氮原子电子效应的影响,其碳碳双键的活性要比普通的烯烃高,因此该反应无需催化剂和添加剂。烯酰胺中的乙酰胺基可以作为离去基团,在特定条件下可以发生碳氮键的断裂,因此该反应无需氧化剂。此外,该合成方法通过氮杂Mannich反应启动反应,因此反应底物不受取代基的限制,可以构建多环体系,该反应的普适性较好,不同种类的C,N-亚甲胺内盐和烯酰胺都可以很好地进行反应,并以良好至优异的产率得到异喹啉并吡唑衍生物。该反应具有较好的应用前景,由已上市药物分子丙磺舒、阿达帕林以及雄诺龙衍生来的烯酰胺,可以与C,N-亚甲胺内盐反应。另外由复杂活性分子烯醇酮、胆甾酮、嘌呤衍生来的烯酰胺也同样能够顺利地进行反应,合成了一系列复杂的基于药物分子的异喹啉并吡唑衍生物。基于发展的方法,作者开发了一条CB1受体拮抗剂III的全新合成路线。从反应的标准产物出发,通过几步转化可以高效地合成CB1受体拮抗剂III,,相比于传统合成方法,合成路线得到缩短,产率也得到了提高。
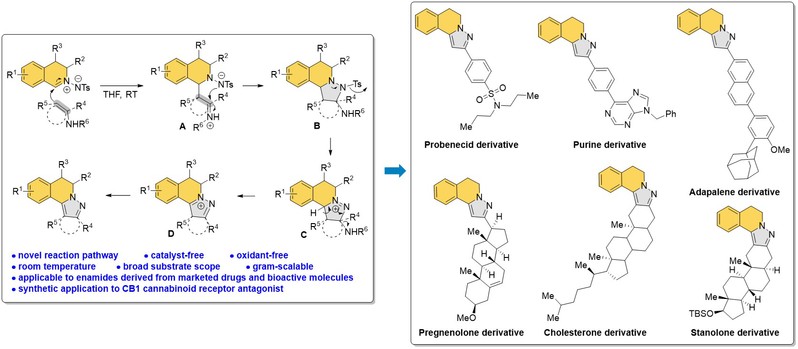
图3. 异喹啉并吡唑骨架的新型合成方法
本文的第一完成单位是中国海洋大学医药学院。王杨副教授为独立通讯作者。文章的共同第一作者是中国海洋大学硕士研究生董浩、张永兴和博士研究生田晓晨。任为武教授为合作作者。该工作得到了中国海洋大学优秀青年科技人才培育基金、山东省自然科学基金、泰山学者青年专家、国家自然科学基金等项目的支持。
文章链接:https://pubs.rsc.org/en/content/articlelanding/2022/gc/d2gc01275h
