| 张峻峰 | 博士 | 教授 | 博士生导师 |
科 室: | 药物分析与药剂学研究 | |||
办公电话: | 电子邮箱: | 2024034@ouc.edu.cn | ||
联系地址: | 山东省青岛市鱼山路5号生命科技大楼 C501 266003 | |||
研究方向: | 1. 纳米生物材料递药系统 2. 代谢功能的体内再生
| |||
个人简介 |
|
|
|
|
中国海洋大学校长,获得国家杰出青年科学基金,教育部****特聘教授,教育部新世纪优秀人才,江苏省“333人才”第二层次培养对象科技领军人才。曾担任医药生物技术国家重点实验室副主任,连续5年入选Elsevier中国高被引学者。主持国家自然科学基金重点项目、科技部973、863、新药创制重大专项等多项科研项目和课题。长期从事高效药物递送系统研究,聚焦基于炎症及相关疾病特别是癌症发病机制的靶向治疗新策略,以病理生理学现象为导向,发展了一系列纳米生物材料递药系统,在肿瘤、炎症性肠病及肝肾纤维化等重大疾病治疗方面取得了显著进展和一系列的原创研究成果。作为主要完成人获得国家自然科学二等奖2项,教育部科学技术奖自然科学一等奖2项;研究成果中1项医用生物材料实现转化应用,2项药物材料进入临床前研究阶段。 | ||||
教育背景 |
|
|
|
|
1993~1995 | 日本京都大学再生医学研究所 | 博士 |
| |
工作经历 |
|
|
|
|
2023~今 | 中国海洋大学 医药学院 | 教授 |
| |
2001~2023 | 南京大学 生命科学学院 | 教授 |
| |
1997~2000 | 新加坡国立大学 | 访问学者 |
| |
学术兼职 |
|
|
|
|
江苏省药物研究与开发协会副理事长 Pharmaceutical Sciences编委
| ||||
承担课程 |
|
|
|
|
学科前沿课(本科生课程) | ||||
研究进展 |
|
|
|
|
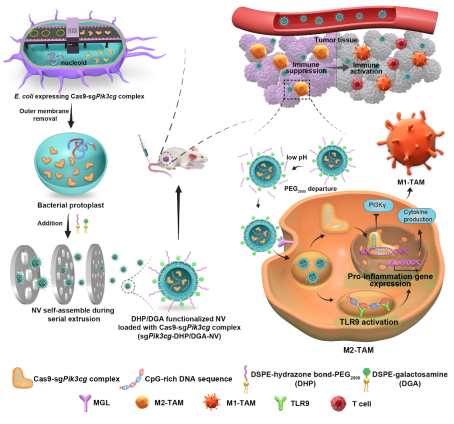
巨噬细胞在炎症肿瘤等重大疾病过程发挥着极其重要的作用,以巨噬细胞为靶标的功能调控始终是生物治疗领域的热点。课题组明确了关键靶标分子,并进一步通过寻找巨噬细胞亚群表面的特征性受体,依据疾病病理特征设计开发了基于多糖聚合物、生物囊泡等不同类型的载体。通过高效靶向输送核酸药物至巨噬细胞进而重塑其表型,在肿瘤、肠炎等重大疾病动物模型上取得了显著疗效。
基于递送系统的巨噬细胞及其在免疫治疗中的应用 脾脏具备丰富的天然血管网络和较大的移植细胞容纳空间,这是脾脏作为其他器官再生位点的优势。然而,脾脏缺乏细胞外基质,而细胞外基质是细胞粘附和生长所必需的。为了细胞更好的存活和生长,脾脏免疫环境的调节是必要的。课题组尝试通过模拟生理/病理微环境对脾脏进行深度改造,并结合细胞移植/组织移植/细胞重编程/基因编辑手段,在小鼠脾内实现了多种复杂器官的再生(肝脏、甲状腺、胰岛),在大动物脾脏中实现了人源胰岛组织的功能性重建,利用相关技术在脾脏外建立了具有减肥功能的耗能组织。
以脾脏为基础的功能器官体内重建 | ||||
代表性成果 | ||||
代表性论文 |
|
|
|
|
2. Mingming Zhao, Xiaohui Cheng, Pingwen Shao, Yao Dong, Yongjie Wu, Lin Xiao, Zhiying Cui, Xuedi Sun, Chuancheng Gao, Jiangning Chen*, Zhen Huang*, Junfeng Zhang*. Bacterial protoplast-derived nanovesicles carrying CRISPR-Cas9 tools re-educate tumor-associated macrophages for enhanced cancer immunotherapy. Nature Communications. 2024;15(1):950. 3. Xiaohui Cheng, Pingwen Shao, XinTong Wang, Juan Jiang, Jiahui Chen, Jie Zhu, Weiming Zhu, Yi Li*, Junfeng Zhang*, Jiangning Chen*, Zhen Huang*. Myeloid-Derived Suppressor Cell Accumulation Drives Intestinal Fibrosis through mCCL6/hCCL15 Chemokine-Mediated Fibroblast Activation. Advanced Science. 2024:e2411711. 4. Lintao Wang, Yajie Sun, Lifang Yang, Shaocong Wang, Chunyan Liu, Yulian Wang, Yiming Niu, Zhen Huang, Junfeng Zhang*, Chunming Wang*, Lei Dong*. Engineering an energy-dissipating hybrid tissue in vivo for obesity treatment. Cell Reports. 2024;43(7):114425. 5. Zhiqian Kang, Chenqi Wang, Fang Shao, Hao Deng, Yanyan Sun, Zhengrong Ren, Wei Zhang, Zhi Ding, Junfeng Zhang*, Yuhui Zang*. The increase of long noncoding RNA Fendrr in hepatocytes contributes to liver fibrosis by promoting IL-6 production. Journal of Biological Chemistry. 2024;300(6):107376. 6. Zhen Xing, Jing Xue, Xindian Ma, Congwei Han, Zhenzhen Wang, Shunhuang Luo, Chunming Wang*, Lei Dong*, Junfeng Zhang*. Intracellular mRNA phase separation induced by cationic polymers for tumor immunotherapy. Journal of Nanobiotechnology. 2022;20(1):442. 7. Chunyan Liu, Lintao Wang#, Mengzhen Xu, Yajie Sun, Zhen Xing, Junfeng Zhang*, Chunming Wang*, Lei Dong*. Reprogramming the spleen into a functioning ‘liver’ in vivo, Gut. 2022;71(11):2325-2336. 8. Yulian Wang, Jiayun Pang, Qingyun Wang, Luocheng Yan, Lintao Wang, Zhen Xing, Chunming Wang* , Junfeng Zhang*, Lei Dong*. Delivering Antisense Oligonucleotides across the Blood-Brain Barrier by Tumor Cell-Derived Small Apoptotic Bodies. Advanced Science. 2021;8(13):2004929. 9. Lintao Wang#, Chunming Wang#*, Zhenzhen Wang, Jingjing Gan, Chunyan Liu, Suhua Xia, Yiming Niu, Dianhua Chen, Junfeng Zhang*, Lei Dong*. Transforming the Spleen into a Liver-like Organ in vivo, Science Advances. 2020;6(24):eaaz9974. 10. Wei He, Jinzhi Xu, Ruoyu Mu, Qiu Li, Da-Lun Lv, Zhen Huang, Junfeng Zhang*, Chunming Wang*, Lei Dong*. High-salt diet inhibits tumour growth in mice via regulating myeloid-derived suppressor cell differentiation. Nature Communications. 2020;11(1):1732. | ||||
获奖 |
|
|
|
|
1. 2024. 国家自然科学二等奖 2. 2012. ****特聘教授 3. 2011. 教育部科学技术一等奖 4. 2010. 国家杰出青年科学基金 5. 2004. 国家自然科学二等奖 6. 2003. 教育部科学技术一等奖 | ||||
项目课题 | ||||
1. 国家自然科学基金重点项目, 2023/01-2027/12,主持。 2. 国家自然科学基金区域合作项目, 2025/10-2028/12,主持。 3. 江苏省自然科学基金,2024/04-2026/03,主持。 | ||||