近日,中国海洋大学医药学院、海洋药物教育部重点实验室李德海教授课题组在真菌来源对醌甲基化物(p-QM)的生物合成与寡聚化方面取得重要进展。相关研究成果以“A methyltransferase molecular switch unlocks para-quinone methide generation and oligomerization(甲基转移酶分子开关实现对醌甲基化物的生成与寡聚化)”为题,发表在国际知名学术期刊《Chemical Science》上。
醌甲基化物(Quinone methides,QMs)是一类具有共轭醌式亚甲基结构的高活性中间体,兼具亲电与亲核特性,广泛应用于有机合成与天然产物生物合成中(图1)。然而,其固有的不稳定性及缺乏可控的生成方法限制了其进一步应用。尤其在生物合成中,尽管邻位醌甲基化物(o-QM)的生成路径已较为明确,但对位醌甲基化物(p-QM)的专一性生成路径仍不清楚。
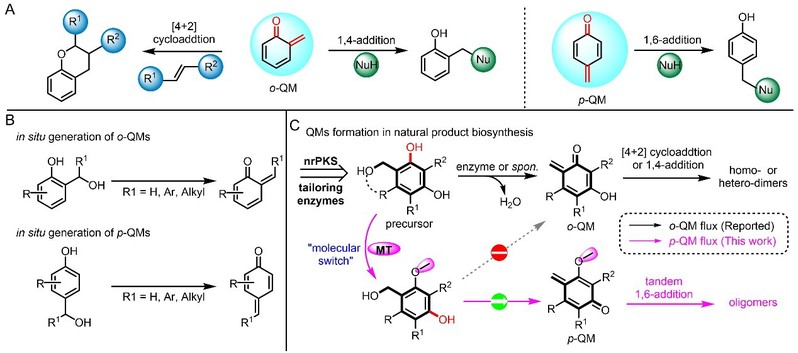
图1. 醌甲基化物(o-QM与p-QM)的结构与反应类型比较
课题组从海洋真菌Mycocitrus zonatus Mcr中鉴定了一个负责p-QM生成的生物合成基因簇(acre)。研究发现,该基因簇编码的非还原性聚酮合酶(AcreA)和短链脱氢酶/还原酶(AcreB)共同合成具有双反应潜力的2,4-二羟基苯甲醇前体。关键的是,一种新型膜依赖性甲基转移酶AcreE能够区域选择性地对该前体的邻位羟基进行甲基化修饰,从而阻断o-QM的生成路径,并引导其专一性地形成p-QM中间体(图2)。该p-QM中间体随后通过迭代的分子间1,6-共轭加成反应,形成一系列结构多样的寡聚产物。
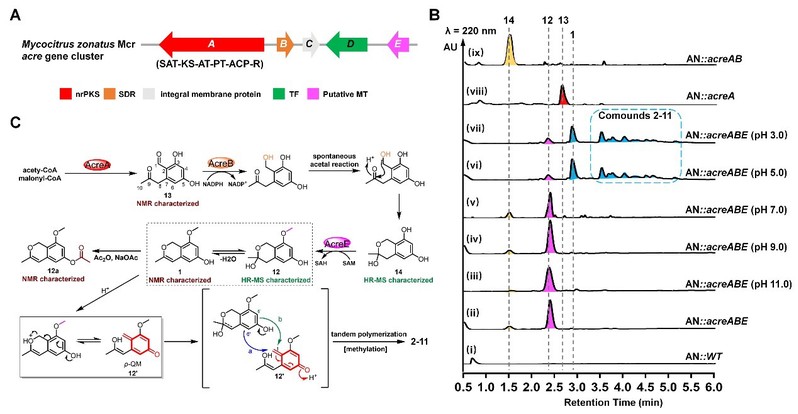
图2. 化合物acrepolyphenols生物合成途径中关键p-QM中间体的生成与寡聚化
该研究首次揭示了一种天然产物生物合成中膜依赖性甲基转移酶通过简单甲基化修饰精准控制反应性中间体命运的新机制。该策略不仅为理解自然界中反应性中间体的调控提供了新视角,也为发展生物启发合成方法学、构建结构多样的p-QM衍生物及开发新型生物基聚合物材料提供了新思路。
本文的第一完成单位是中国海洋大学医药学院,中国海洋大学医药学院李德海教授与张峻峰教授为共同通讯作者。中国海洋大学医药学院博士后马传腾、毕业博士生张真真及博士后王文雪为共同第一作者。该工作得到了国家重点研发计划、青岛海洋科技中心科技创新项目、海南省重点研发计划、山东省泰山学者特聘专家计划、国家自然科学基金等项目的支持。
文章链接:https://doi.org/10.1039/D5SC06912B
