
近日,中国海洋大学医药学院、海洋药物教育部重点实验室邵长伦课题组和卢玲课题组共同合作,在海洋来源HIF-1α抑制剂作为癌症治疗候选药物开发领域取得重要进展,相关研究成果以“Discovery of Oral Natural Benzofuranoid p-Terphenyl Derivative CHNQD-03301 as a Potent Hypoxia-Inducible Factor-1α Signaling Inhibitor for Cancer Therapy”(《口服天然苯并呋喃对三联苯衍生物CHNQD-03301作为缺氧诱导因子-1α信号通路的强效抑制剂用于癌症治疗的发现》)为题发表在药物化学顶尖期刊Journal of Medicinal Chemistry(10.1021/acs.jmedchem.5c01859)上。
癌症仍然是全球主要的公共卫生问题,也是导致全球疾病负担的主要因素。实体瘤常处于缺氧微环境中,缺氧诱导因子-1α(HIF-1α)是调控肿瘤适应缺氧、促进血管生成、增强侵袭转移及产生耐药性的关键转录因子。因此,HIF-1α被认为是极具潜力的抗肿瘤药物靶点。然而,目前已报道的HIF-1α抑制剂大多活性有限或成药性差,临床上尚无批准上市的HIF-1α抑制剂用作癌症治疗。海洋天然产物因其独特的化学结构和生物活性,是发现潜在抗癌药物重要来源。
研究团队从海洋真菌Aspergillus candidus来源的天然产物terphenyllin出发,通过活性筛选发现其对HIF-1α信号通路具有抑制作用。设计合成并构建了三联苯库,对该类化合物的活性和构效关系(SAR)进行了评价。发现了一种口服天然苯并呋喃对三联苯衍生物 CHNQD-03301(IC₅₀ = 10.97 nM),它带有罕见的丙酮叉基团,是一种具有强效活性的 HIF-1α信号抑制剂。
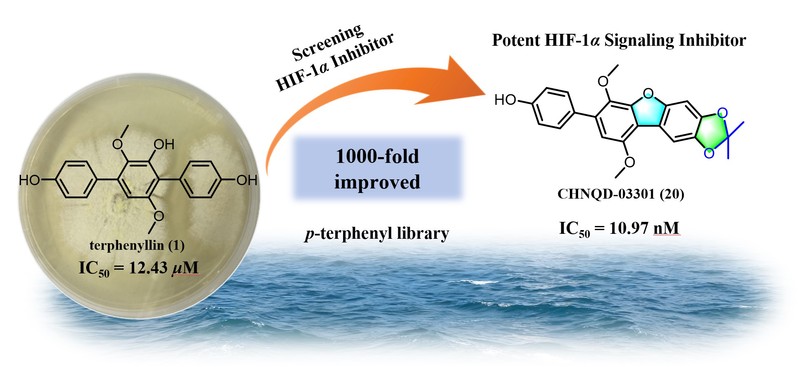
图1. HIF-1α抑制剂的发现
从机制上讲,该化合物促进了HIF-1α蛋白的蛋白酶体降解,显著抑制其蛋白水平及下游靶基因(如CA9、VEGF、REDD1等)的表达,且该作用不依赖于VHL蛋白。进一步研究表明,在斑马鱼模型中,它能够逆转 HIF 积累诱导的血管生成,并减轻 HIF 诱导的红细胞增多表型。
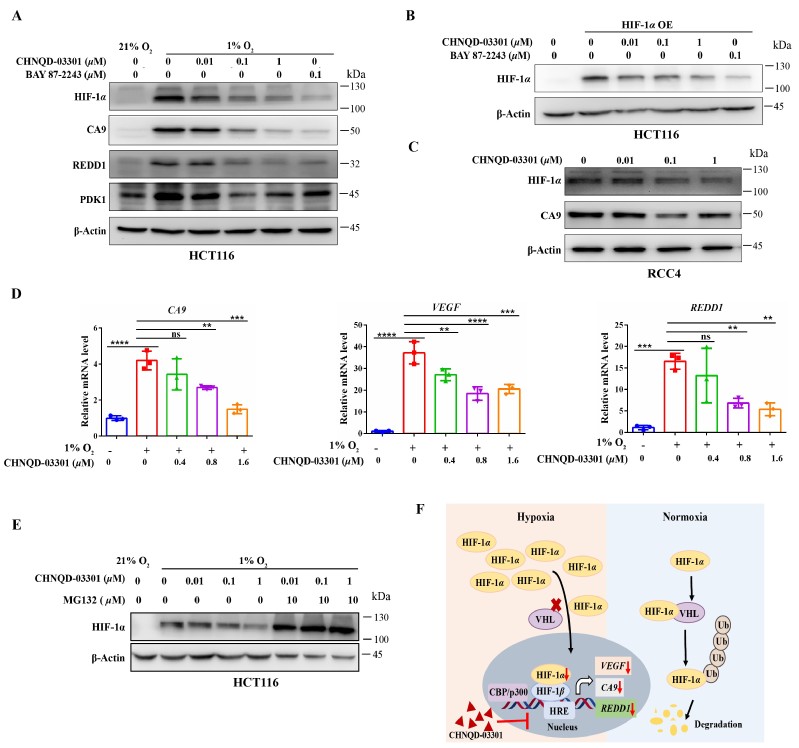
图2. 化合物CHNQD-03301作用机制研究
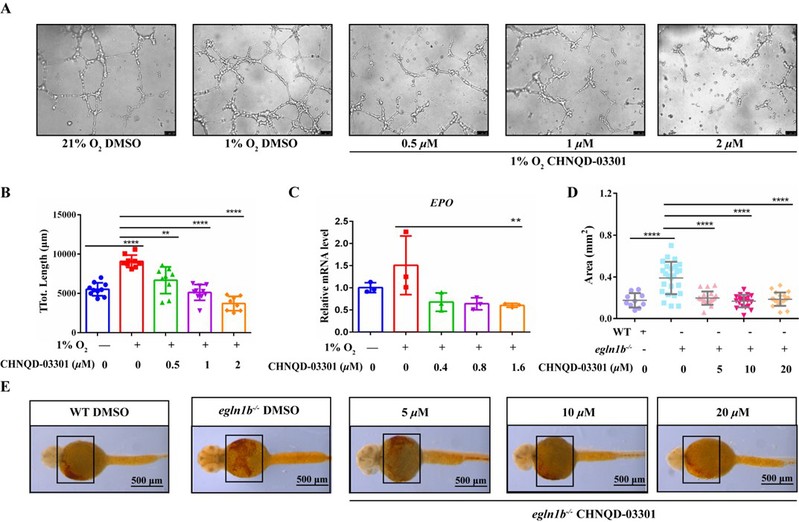
图3. 化合物CHNQD-03301在斑马鱼模型中的活性研究
在 HCT116 异种移植模型和 MB49 同种异体移植模型中,CHNQD-03301 以 1 mg/kg 的剂量(口服)分别显著抑制了肿瘤生长(肿瘤生长抑制率 = 51.0% 和 52.0%)。同时,CHNQD-03301 表现出良好的药代动力学特性(F=94.5%)和安全性(MTD>100mg/kg)。这些数据均表明该化合物CHNQD-03301是一种有前景的口服 HIF-1α 信号抑制剂,可用于癌症治疗的进一步开发。
中国海洋大学为第一完成单位,邵长伦教授和卢玲副教授为通讯作者,医药学院博士生毕业生王翠芳、硕士毕业生崔晓楠和博士生吕柳霞为共同第一作者,王文慧、荆倩倩、尹俊娜、曹西珍以及魏美燕副教授为文章共同作者。相关工作得到国家自然科学基金、山东省青岛海洋科学与技术中心专项资金、崂山实验室自由探索项目等项目的资助。
文章链接:https://doi.org/10.1021/acs.jmedchem.5c01859
