王德财 | 博士 | 副教授 | 硕士生导师 | ||
科室: | 海洋药物作用机制与新靶标发现 | ||||
办公电话: | 15255613643 | 电子邮箱: | wangdecai@ouc.edu.cn | ||
联系地址: | 山东省青岛市鱼山路5号中国海洋大学,生命科技楼C411, 266003 | ||||
研究方向: | 1. 食物-微生物-宿主互作网络及调控机制 2. 肠道炎症小体通路的功能及调控机制 3. 翻译后修饰在肠道疾病中的功能及作用机制 | ||||
个人简介 | |||||
王德财,博士,2026年3月加入中国海洋大学医药学院开展独立研究工作。主要从事肠道感染与炎症性疾病的致病机制研究,聚焦“食物-微生物-宿主”互作网络,综合运用分子、细胞、组织、类器官及动物模型等多维度研究体系,系统解析肠道炎症小体信号激活所介导的细胞因子通路与细胞焦亡通路的新功能及其翻译后调控机制,致力于阐明疾病起始和进展的核心规律,为新型靶点识别与干预策略开发奠定基础。目前主要贡献包括:(1)系统阐明肠道模式受体NLRP6的翻译后修饰激活炎症小体通路的分子机制;(2)发现并阐明食物多肽激活细胞焦亡执行者GSDMD的非死亡剪切形式从而诱导小肠食物耐受的分子机制;(3)发现并阐明RNA解旋酶DHX9在细胞核内调控I型干扰素通路的分子机制;(4)发现并阐明食物组分抑制炎症小体信号限制肠道炎症进展的分子机制。近年来主持国家自然科学基金青年基金项目和中国博士后科学基金面上项目。相关研究成果以第一或共第一作者身份发表于Cell,Cell Host & Microbe,Science Advances等国际高水平学术期刊。 | |||||
2016.09-2022.11 | 生命科学与医学部 | 细胞生物学 | 硕博连续 | ||||||||||||||||||||||||||
2012.09-2016.07 | 电子科技大学 | 生命科学与技术学院 | 生物技术 | 学士 | |||||||||||||||||||||||||
工作经历 | |||||||||||||||||||||||||||||
2026.03.10至今 | 中国海洋大学 | 医药学院 | 青年英才二层次 | ||||||||||||||||||||||||||
2023.08-2026.02 | 合肥综合性国家科学中心 | 大健康研究院 | 博士后 | ||||||||||||||||||||||||||
2022.12~2023.07 | 中国科学技术大学 | 微尺度国家研究中心 | 助理研究员 | ||||||||||||||||||||||||||
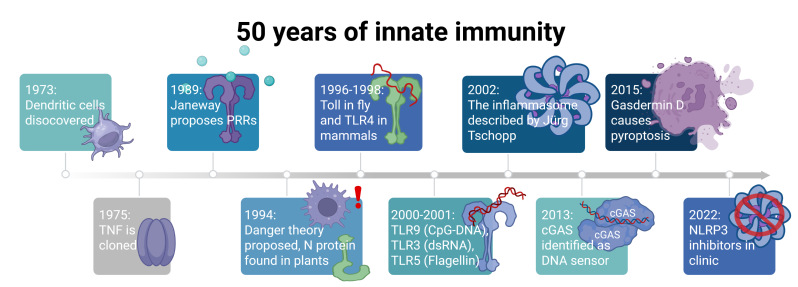
研究进展 一、固有免疫里程碑事件:炎症小体及其介导的细胞焦亡与细胞因子信号 固有免疫系统由组织屏障、固有免疫分子和固有免疫细胞组成,是机体抵御病原入侵的第一道防线。该系统主要依赖模式识别受体(PRRs)识别病原体相关分子模式(PAMPs)和损伤相关分子模式(DAMPs),其功能异常与感染性疾病、自身免疫病、炎症性疾病及肿瘤等多种病理状态密切相关。我们正进入一个靶向固有免疫受体及下游信号,治疗感染性和炎症性疾病及癌症领域具有巨大潜力的时代。 1973 年树突状细胞的发现为固有免疫与适应性免疫的关联奠定基础;1989 年查尔斯・詹韦(Charles Janeway)革命性提出模式识别受体假说,标志固有免疫研究真正意义上进入分子时代。20 世纪90 年代至21 世纪初,固有免疫研究迎来历史性突破:1997 年人类Toll 样受体(TLRs)同源物被鉴定;1998 年TLR4 被确认为脂多糖(LPS)受体,研究荣获2011 年诺贝尔生理学或医学奖;2002 年炎症小体(inflammasome)概念正式提出,揭示了其在促炎因子激活中的核心作用;2013 年环鸟苷酸-腺苷酸合成酶(cGAS)的发现,揭示了DNA感知机制。随后2015年细胞焦亡(Pyroptosis)执行者Gasdermin D的发现以及NLRP3抑制剂进入临床试验强调了炎症小体信号通路在固有免疫当中的核心地位。这一系列突破逐步构建了固有免疫的分子调控网络,使其成为抗感染、抗炎及抗肿瘤治疗的重要靶点。
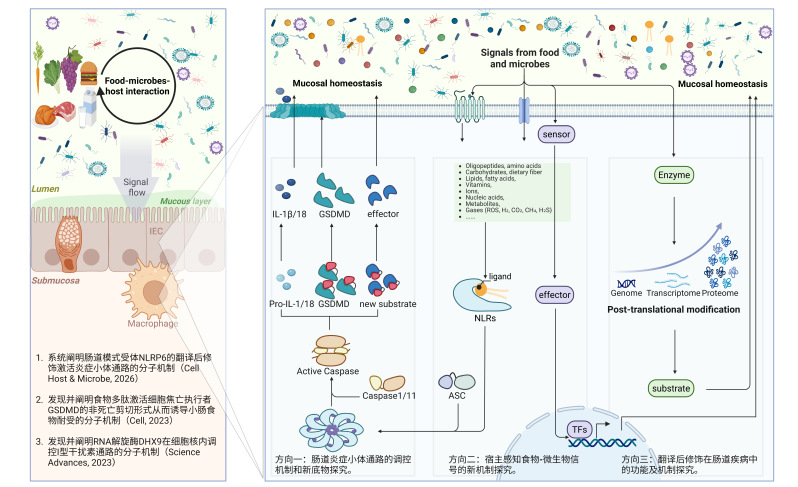
肠道是人体与外界环境接触最广泛的黏膜屏障之一,肠道上皮细胞与固有免疫细胞持续暴露于由共生微生物、潜在病原体及食物组分构成的复杂微环境中,依靠精密免疫监测机制维系肠道稳态。随着工业发展与生活方式的改变,肠炎和肠道感染发病率逐年攀升,已严重威胁国民健康并加重社会医疗负担。据预估,2025年我国炎症性肠病(IBD)患者将达150万人;而肠道病毒感染的危害同样严峻,轮状病毒感染每年引发全球2.6 亿腹泻病例,造成约13万5岁以下儿童死亡;诺如病毒每年致死约20万人死亡。研究表明,肠道食物-微生物-宿主的互作网络是调控宿主抗感染免疫、维持肠道黏膜稳态的核心机制。解析三者相互作用,不仅能为炎症性肠病与肠道感染发病机制提供理论见解,也将为研发基于饮食干预的肠道疾病预防与治疗策略开辟新途径。
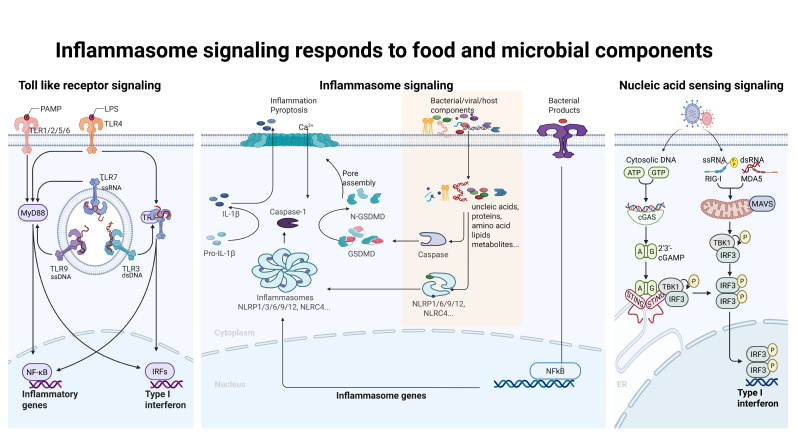
目前固有免疫研究主要聚焦在Toll 样受体信号(Toll like receptor signaling)、Nod样受体介导的炎症小体信号(Inflammasome signaling)和MAVS/cGAS介导的感知信号(MAVS/cGAS signaling)三大信号通路。其中Nod样受体能特异识别食物或微生物组分,激活NLRs-ASC-Caspase1/11-IL1 family/GSDMD经典炎症小体通路,在抗感染和炎症调控中至关重要。肠道上皮细胞高表达NLRP6和NLRP9,肠道固有免疫细胞高表达NLRP1、NLRP3、NLRC4和NLRP12等受体。两者均组成或诱导型高表达ASC、Caspase1、Caspase11、IL1、IL18和GSDMD等下游关键元件。2022年以来,全球针对炎症小体通路治疗炎症性疾病的抑制剂临床试验爆发式增长。然而,肠道特异炎症小体通路的激活和调控机制仍不明确。因此深入揭示食物-微生物信号调控肠道炎症小体的分子机制机及其新功能,将为阐明肠道感染与炎症疾病机理、研发组织特异性靶向药提供重要理论基础。 三、我的研究进展和未来研究方向: 近年来,我们围绕肠道炎症小体通路和翻译后修饰系统,在肠道食物耐受和抗感染免疫领域取得了突破性进展:1.我们发现在小肠前端半胱天冬氨酸蛋白酶Caspase3/7能够直接识别蛋白质降解形成的多肽分子被激活,活化的Caspase3/7切割细胞焦亡执行者GSDMD产生新型的13 kDa非死亡剪切形式。该剪切转位进入细胞核调控二类分子MHCII的表达并维持小肠前端Tr1细胞类群,最终介导食物耐受的形成。该研究证明了GSDMD的差异性切割是控制小肠免疫与耐受的调控枢纽(Cell, 2023)。2.我们发现细胞核定位的RNA解旋酶DHX9结合转录因子STAT1,调控I型干扰素通路下游STAT1介导ISGs基因的转录过程。该发现首次在体内证实了DHX9的抗病毒作用并解析了核定位DHX9的非胞质感受器的分子机制(Science Advances,2023)。3.我们发现了NLRP6的第一个翻译后写手,首次揭开了单泛素化在NLR家族蛋白激活中的潜在关键作用,并提出了NLRP6炎症小体活化的“双保险模型”:即通过K680-687位点驱动构象转变依赖的寡聚,和通过K115-130引发空间位阻维持胞质定位,两者协同确保炎症小体的高效、精准激活。这一发现深化了对蛋白质翻译后修饰调控免疫信号的理解,也为未来靶向NLRP6通路调控肠道炎症及相关药物优化提供了重要的理论依据(Cell Host & Microbe, 2026)。今后我们将继续以肠道巨噬细胞与上皮细胞中的炎症小体通路及翻译后修饰系统为核心,围绕肠道感染与炎症性疾病的致病机制开展深入研究:1.解析食物-微生物-宿主互作的新通路与调控机制;2.探索肠道炎症小体通路的调控机制及其新功能;3.阐明翻译后修饰系统在肠道疾病中的功能及作用机制。
| |||||||||||||||||||||||||||||
代表性论文 | |||||||||||||||||||||||||||||
1. Wang D*, Chen X*, Sui K, Wang A, Li R, Zhou W, Zhu X, Hua Y, Yuan S, Zhou R, Dong F, Wang K, Zheng J, Zhu S. UBE2O-mediated monoubiquitination licenses NLRP6 inflammasome activation in the intestine. Cell Host & Microbe. 2026 Jan 14;34(1):86-102.e8. doi: 10.1016/j.chom.2025.12.009. Epub 2026 Jan 6. PMID: 41500221. | |||||||||||||||||||||||||||||
2. He K*, Wan T*, Wang D*, Hu J*, Zhou T, Tao W, Wei Z, Lu Q, Zhou R, Tian Z, Flavell RA, Zhu S. Gasdermin D licenses MHCII induction to maintain food tolerance in small intestine. Cell. 2023 Jul 6;186(14):3033-3048.e20. doi: 10.1016/j.cell.2023.05.027. Epub 2023 Jun 15. PMID: 37327784. | |||||||||||||||||||||||||||||
3. Ren X*, Wang D*, Zhang G*, Zhou T, Wei Z, Yang Y, Zheng Y, Lei X, Tao W, Wang A, Li M, Flavell RA, Zhu S. Nucleic DHX9 cooperates with STAT1 to transcribe interferon-stimulated genes. Science Advances. 2023 Feb 3;9(5):eadd5005. doi: 10.1126/sciadv.add5005. Epub 2023 Feb 3. PMID: 36735791. | |||||||||||||||||||||||||||||
4. Li R, Zan Y, Wang D, Chen X, Wang A, Tan H, Zhang G, Ding S, Shen C, Wu H, Zhu S. A mouse model to distinguish NLRP6-mediated inflammasome-dependent and -independent functions. Proc Natl Acad Sci U S A. 2024 Feb 6;121(6):e2321419121. doi: 10.1073/pnas.2321419121. Epub 2024 Jan 30. PMID: 38289959. | |||||||||||||||||||||||||||||
5. Ren X, Liu Q, Zhou P, Zhou T, Wang D, Mei Q, Flavell RA, Liu Z, Li M, Pan W, Zhu S. DHX9 maintains epithelial homeostasis by restraining R-loop-mediated genomic instability in intestinal stem cells. Nat Communications. 2024 Apr 9;15(1):3080. doi: 10.1038/s41467-024-47235-2. PMID: 38594251. | |||||||||||||||||||||||||||||
6. Zhao K, Wang D, Zhao X, Wang C, Gao Y, Liu K, Wang F, Wu X, Wang X, Sun L, Zang J, Mei Y. WDR63 inhibits Arp2/3-dependent actin polymerization and mediates the function of p53 in suppressing metastasis. EMBO Reports. 2020 Apr 3;21(4):e49269. doi: 10.15252/embr.201949269. Epub 2020 Mar 4. PMID: 32128961. | |||||||||||||||||||||||||||||
7. Wang A, Tao W, Tong J, Gao J, Wang J, Hou G, Qian C, Zhang G, Li R, Wang D, Ren X, Zhang K, Ding S, Flavell RA, Li H, Pan W, Zhu S. m6A modifications regulate intestinal immunity and rotavirus infection. Elife. 2022 Jan 31;11:e73628. doi: 10.7554/eLife.73628. PMID: 35098923. | |||||||||||||||||||||||||||||
8. Zhao K, Yang Y, Zhang G, Wang C, Wang D, Wu M, Mei Y. Regulation of the Mdm2-p53 pathway by the ubiquitin E3 ligase MARCH7. EMBO Reports. 2018 Feb;19(2):305-319. doi: 10.15252/embr.201744465. Epub 2018 Jan 2. PMID: 29295817. | |||||||||||||||||||||||||||||
9. Yang Y, Wang C, Zhao K, Zhang G, Wang D, Mei Y. TRMP, a p53-inducible long noncoding RNA, regulates G1/S cell cycle progression by modulating IRES-dependent p27 translation. Cell Death & Disease. 2018 Aug 30;9(9):886. doi: 10.1038/s41419-018-0884-3. PMID: 30166522. | |||||||||||||||||||||||||||||
项目课题
| |||||||||||||||||||||||||||||